Auch bei der Maine Coon hat sich im Laufe ihrer Zucht das Vorhandensein diverser erblich bedingter katzentypischer Krankheiten herausgestellt. Für einige dieser Krankheiten gibt es bei PawPeds ein Gesundheitsprogramm. Die Züchter sind angehalten, ihre Tiere auf diese Erbkrankheiten untersuchen zu lassen und die Ergebnisse bei PawPeds in der Datenbank eintragen zu lassen. So kann dann jeder Züchter und auch Liebhaber Auskunft über die Gesundheit vorhergehender Generationen bekommen, Züchter können damit Rückschlüsse auf zu erwartende Kitten ziehen. |
|
Hypertrophe Kardiomyopathie (HKM bzw. HCM) |
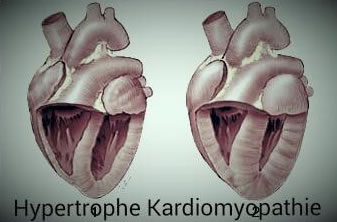 |
Ein Tier mit Hypertrophe Kardiomyopathie erscheint nach außen gesund. Es wird wahrscheinlich zu einem nicht vorhersehbaren Zeitpunkt den plötzlichen Herztod sterben. Eine HCM kann mit gutem Erfolg medikamentös eingestellt, jedoch in der Regel nicht geheilt werden. Regelmäßige Herzuntersuchungen - etwa alle 1-2 Jahre per Ultraschall zur sicheren Abklärung sind hier das Optimum. |
Genmutationen: |
Merke:
Das Vorliegen einer Mutation bei einer Katze bedeutet nicht automatisch, dass sie auch an einer HCM erkranken wird! Schon einige Monate nach Markteinführung des ersten Gentests und der großen Anfangseuphorie kamen berechtigte Zweifel an der Voraussagekraft des Gentests auf. |
| Es wurden auf einem Gen (kardiales MYBPC3) nur drei Mutationen beschrieben: |
- A31P —> Nur jede fünfte im Gentest positive Katze war auch herzkrank!
- A74T —> Dreiviertel der an HCM erkrankten Katzen waren genetisch unauffällig!
- R820W
|
Verhältnis von HCM-Genotyp zu Phänotyp: „Da stimmt etwas nicht.“ |
|
Eine neuere bemerkenswerte Publikation von Frau Schinner aus dem Jahre 2008 belegt den Zweifel an dem Wert der HCM-Gentests für hiesige Katzen. |
Da der A74T-Polymorphismus des MYBPC3-Gens in dieser Studie wie auch in anderen Erhebungen genauso häufig bei Maine Coon wie bei anderen Katzenrassen vorkommt, kann es sich hier nicht um eine Maine Coon-spezifische Mutation handeln. Zudem gibt es keine Verstärkung des Erkrankungsgrades, wenn A31P und A74T bei einem Individuum gleichzeitig auftreten. Man kann also davon ausgehen, dass es sich bei der HCM um eine genetisch komplexe Erkrankung handelt. |
Herzultraschall |
Die Echokardiografie (Herzultraschall) mit ihren verschiedenen Applikationsmöglichkeiten (Doppler, Tissue-Doppler, Strain und Strain/rate) ist die beste Methode, eine Hypertrophie der Herzmuskulatur phänotypisch nachzuweisen. Natürlich gibt es auch andere kardiologische Verfahren, von denen das Abhören des Herzens sehr wichtig ist. Das EKG und die Röntgenuntersuchung sind im Rahmen einer Früherkennung der HCM eher unbrauchbar. Die Ultraschalluntersuchung ist bei Vorliegen einer Hypertrophie sehr sensitiv, kann aber bei Katzen ohne Befund die genetische Belastung und das spätere Auftreten nicht ausschließen. |
Grundvoraussetzung – neben der Erfahrung des Untersuchers – sind Schallköpfe mit hoher Auflösung (7,5-10 MHz) und hoher Bildfrequenz. Die Hypertrophie kann sich als symmetrische und asymmetrische Verdickung der Herzwände und Papillarmuskel darstellen. Fast immer ist nur die linke Herzkammer davon betroffen. Grundlage der Diagnostik ist die Messung der Wanddicke in Diastole, der Herzphase der Muskelerschlaffung. Zunächst wird der Herzmuskel im 2-dimensionalen Bild in mehreren Ebenen beurteilt. Dann folgt eine M-Mode-Messung der diastolischen Wandstärke in den definierten Standardebenen. Ist die Hypertrophie symmetrisch verteilt, lassen sich die Wandstärkenzunahmen messen und klassifizieren. Grenzwert für eine normale Wanddicke ist 5,5 mm. Zwischen 5,5 und 6,0 mm sprechen wir von einem zweifelhaften (equivocal) Befund. Das hat damit zu tun, dass es in der Literatur zwei verschiedene Empfehlungen für die Normalwerte der Herzwände bei der Katze gibt. |
Empfehlungen für die Gesundheitsvorsorge |
Die veterinärmedizinische Genforschung hat trotz respektabler Erfolge es leider noch nicht geschafft, einen Gentest zu bieten, der aus züchterischer Sicht von Wert wäre. Für Zuchttiere ist die regelmäßige Ultraschalluntersuchung des Herzens zu empfehlen. Aus juristischen Gründen (§11b TschG) sollte damit vor dem ersten Zuchteinsatz begonnen werden. Danach empfehlen wir eine Wiederholung in 1- bis 2-jährigem Abstand. Die Kontrollabstände hängen vom jeweiligen Ergebnis ab. |
Therapie der HCM |
Es gibt kein Medikament, welches die Tendenz zur Hypertrophie aufhält. Da Stauungen, insbesondere aber Hyperkoagulabilität und Thrombenbildung des Blutes nur im Ultraschall zu erkennen sind, ist diese Untersuchung therapiebegleitend durchzuführen. |
|
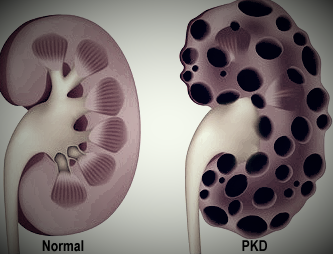
Polyzystrische Nierenerkrankung |
 |
|
Die Polyzystische Nierenerkrankung (PKD) muss unterschieden werden von Nierenzysten (Cystic Renal Disease). Bei beiden entstehen Zysten in den Nieren, aber nur bei der PKD wird die Funktion der Nieren mit dem Wachstum der Zysten mehr und mehr eingeschränkt. Der Verlauf der PKD ist medikamentös einstellbar, aber letztendlich tödlich. Ein Gentest für Perserkatzen und Perserabkömlinge, der nicht für Maine Coon validiert ist, ist vorhanden. Eine regelmäßige Ultraschalluntersuchung der Nieren ist immer noch das Optimum, um potentielle Probleme zu beobachten. |
|
In einer 2013 Veröffentlichten 8jährigen Studie mit teilnehmenden Maine Coons aus der Schweiz, Deutschland und anderen Europäischen Ländern, wurde festgestellt, dass es einzelne Zysten schon bei Jungtieren (bei 7 von 187) gibt, die aber weder PKD darstellen, noch mit dem PKD1 Gentest nachgewiesen werden können. Bei 10 der getesteten Tiere wurde eine Chronische Nierenerkrankung (Chronic Kidney Disease, CKD) festgestellt, die aber wiederum nichts mit Zysten zu tun hat. |
|
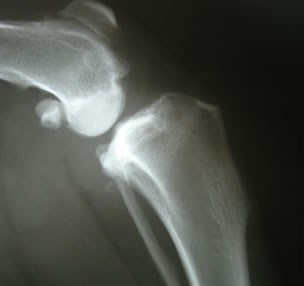
Hüftgelenksdysplasie, Ellenbogendysplasie und Patellaluxation |
 |
|
Bei schnellwachsenden großen, schweren Rassen kann es in der Wachstumsphase zu Komplikationen in den Gelenken kommen. Diagnostiziert werden sie mittels Röntgenuntersuchung der Hüften und Gelenke. Da spezifisches HD-Röntgen vielfach von den Haustierärzten nicht geleistet wird, sollte ein Facharzt für Orthopädie hinzugezogen werden. Operative Hilfe ist möglich, jedoch bei Katzen nicht immer notwendig. |
|
|
Spinale Muskelatrophie |
 |
|
Die Spinale Muskelatrophie (SMA) ist eine Erkrankung der Nervenzellen. Sie verursacht Lähmungserscheinungen. Durch einen Gentest kann der Status bezüglich SMA eindeutig feststellt werden. Die Vererbung der SMA folgt einem autosomal rezessiven Erbgang mit variabler Ausprägung der Symptome. Dies bedeutet, dass die Erkrankung nur bei reinerbig betroffenen Tieren (SMA/SMA) auftritt und daher beide Elterntiere Anlageträger sein müssen. |
|
Symptome |
Betroffene Katzen zeigen erste klinische Anzeichen im Alter zwischen 12 und 15 Wochen, die mit einer zunehmenden Muskelschwäche und Muskelschwund verbunden sind, sowie mit einer Degeneration der spinalen Motorneurone. Beim Stehen können die Hinterpfoten in einem Winkel von 30° – 40° nach außen zeigen - eine Körperhaltung, die vermutlich eingenommen wird, um trotz der Schwäche der proximalen Muskeln eine stabile Haltung zu erreichen. |
Bei einigen zwischen 6 und 12 Monate alten Kitten wurde eine vermehrte Schmerzempfindlichkeit unterhalb des Thorax-Lendenbereiches beobachtet, die sich danach wieder zurückbildete. Bei einigen der betroffenen Jungkatzen wurde eine erschwerte Atmung beobachtet, und alle setzten oder legten sich öfter hin, wenn sie einen Raum durchquerten. |
| Zu den allgemeinen Symptomen gehören: |
- Schwächung der Hinterbeine
- feine Muskelzuckungen
- Eingeschränkte Fähigkeit zu Springen und Landen (Alter von 5 Monaten)
- Gangbild zeigt ein Schwanken der hinteren Körperteile
- leicht erhöhte Aktität der Kreatinphosphokinase (705-964 IU/l, Normalwert < 452 IU/l); als Hinweis für eine leichte Skelettmuskelfaserdegeneration
- Auffällige elektromyographische Aktität an den hinteren Extremitätenmuskeln, den Glutäalmuskeln, den epaxialen Muskeln am thorakolumbalen Übergang
- deutlicher Verlust der großen Motorneurone (Zellleib größer als 100 Mikrometer) der Vorderhörner in allen Ebenen des Rückenmarks
|
Zuchtrelevanz |
Da mischerbige Anlageträger nicht erkranken, besteht vor allem bei wertvollen Zuchttieren keine zwingende Notwendigkeit, diese Tiere umgehend aus der Zucht zu nehmen, es muss aber genau darauf geachtet werden, dass nicht mit einem Anlageträger angepaart wird. Alle Nachkommen aus einer Anpaarung N/SMA x N/N mit denen weiter gezüchtet werden soll müssen gestestet werden, da diese wieder Anlageträger sein können. |
|
Pyruvatkinase Defizienz (PKdef) |
Die Pyruvat-Kinase-Defizienz (PKdef) ist eine erbliche Störung der Glykolyse - dem zentralen Prozess beim Abbau aller Kohlenhydrate. Die Erkrankung hat erhebliche Auswirkungen auf den Energiestoffwechsel der Zelle, insbesondere der Erythrozyten (rote Blutkörperchen). Da Erythrozyten keine Mitochondrien (Zellbestandteile, in denen energiereiche Moleküle gebildet werden) enthalten, müssen sie die notwendige Energie für ihren Stoffwechsel auf andere Weise erzeugen - mittels Glykolyse. Hierbei spielt das Enyzm Pyruvatkinase eine entscheidende Rolle. Fehlt dieses Enzym, können die Erythrozyten ihren Stoffwechsel nicht aufrecht erhalten, und es kommt zu schwerwiegenden Funktionsstörungen, die zur Hämolyse (Auflösung der roten Blutkörperchen) führen. |
Symptome |
Durch die verkürzte Lebensdauer der Erythrozyten entsteht durch deren verstärkten Abbau in der Milz und durch die Hämolyse eine chronische Anämie (Blutarmut). Da der Organismus in der Lage ist, recht schnell Erythrozyten nachzuliefern, ist die Anämie häufig nur intermittierend (mit Unterbrechungen) feststellbar. In der Regel werden anfangs keinerlei Symptome bei der betroffenen Katze feststellbar sein, da aufgrund des langsamen Krankheitsverlaufes die Katze in der Lage ist, sich der Anämie anzupassen. Die ersten Symptome lassen sich in einem Alter zwischen sechs Monaten und fünf Jahren feststellen. Dazu gehören leichte Lethargie, Appetitlosigkeit, Durchfall, blasse Schleimhäute, stumpfes Fell, Gewichtsverlust und Gelbsucht. Die Anämie selbst ist gekennzeichnet durch Makro- und Retikulozytose (erhöhtes Vorkommen von unreifen Vorläuferzellen der Erythrozyten), Hyperglobulinämie, Lymphozytose, Hyperbilirubinämie und hohen Leberenzymwerten. Bei bestehender Retikulozytose sollte immer eine Untersuchung auf die Pyruvat-Kinase-Defizienz durchgeführt werden. |
Therapeutische Maßnahmen sind zurzeit nicht möglich. In einer akuten Krise ist eine Bluttransfusion das einzige Mittel, um das Leben des Tieres zu retten. Hierfür ist die Kenntnis der Blutgruppe wichtig. Um den verstärkten Abbau der Erythrozyten in der Milz zu unterbinden, kann eine Splenektomie (Entfernung der Milz) in Betracht gezogen werden. |
Ursache |
Ursache der Pyruvat-Kinase-Defizienz ist eine Mutation im PKLR-Gen. Dieses Gen liegt in zwei Kopien vor, von denen eine vom Vater und eine von der Mutter vererbt werden. Die Pyruvat-Kinase-Defizienz wird autosomal rezessiv vererbt. Das bedeutet, dass sowohl männliche, wie auch weibliche Tiere gleichermaßen betroffen sind und nur Tiere erkranken können, wenn beide Genkopien die Mutation tragen. Das kann nur dann passieren, wenn sowohl Vater als auch Mutter die PK-verursachende Mutation tragen und beide die Mutation an den Nachkommen vererbt haben. |
Folgende Genotypen sind möglich: |
| N/N |
—> |
Das Tier trägt nicht die PK-verursachende Mutation. Es ist reinerbig für die Normalkopie des Gens. Es wird als N/N ( normal = clear) bezeichnet und wird nicht erkranken. |
| N/PK |
—> |
Tiere, die in nur einer Genkopie die Mutation tragen werden als N/PK (Anlageträger = carrier) bezeichnet. Sie sind mischerbige Träger der Mutation und erkranken nicht. Sie können aber die PK-Anlage mit 50%iger Wahrscheinlichkeit weitervererben. |
| PK/PK |
—> |
Tiere, bei denen die PK-verursachende Mutation in beiden Genen auftritt, werden im Befundbericht als PK/PK ( betroffen = affected) bezeichnet. Sie sind reinerbige Träger der Mutation und erkranken an PK. Sie vererben die PK-Anlage mit 100%iger Wahrscheinlichkeit an die Nachkommen. |
|
Zuchtrelevanz |
Für die Zucht ist entscheidend, dass Anlageträger (tragen ein mutiertes Gen und ein normales Gen) zwar selbst nicht erkranken, die PK-Erbanlage aber mit einer Wahrscheinlichkeit von 50% an ihre Nachkommen weitergeben. Bei der Verpaarung von zwei Anlageträgern besteht also die Gefahr, dass ein Teil der Nachkommen von der Erkrankung betroffen ist. Anlageträger müssen aber nicht automatisch aus der Zucht ausgeschlossen werden. Verpaart man diese mit einem N/N Tier (trägt zwei normale Genkopien), können die Nachkommen nur aus nicht betroffenen N/N-Tieren und nicht erkrankenden Anlageträgern N/PK bestehen. |
Für den Züchter ist das frühzeitige Wissen um die genetische Veranlagung seiner Tiere von besonderer Bedeutung. Der Gentest gibt eine eindeutige Auskunft über das Vorliegen der genannten Mutation. Der Züchter kann so unter Berücksichtigung der Information über die genetische Veranlagung mögliche Anpaarungen genau planen. |
|
|